Ayt kimya Fonksiyonel Bileşikler 2
KETONLAR
Karbonil grubuna iki tane alkil grubunun bağlanmasıyla oluşur. Ketonların genel formülü,
 veya RCOR şeklindedir.
veya RCOR şeklindedir.
- Ketonlarda alkil grupları aynı ise basit keton, farklı ise karışık ketondur.

Basit keton Karışık keton
Ketonların İsimlendirmesi
- Alkil gruplarından sonra keton kelimesi getirilir.
- Türediği hidrokarbondan sonra –ON eki getirilir.

Ketonların Özellikleri
- Ketonların az sayıda C atomu taşıyan molekülleri suda çözünürler. Büyük moleküllü ketonlar katıdır.
- Ketonlar yükseltgenmezler. Zorlanırsa CO2 ve H2O ya parçalanırlar.
- Ketonlar polimerleşme reaksiyonu vermezler. (Aseton hariç)
- Ketonlar katılma reaksiyonu verirler.
Hidrojen katılması (İndirgenme Reaksiyonu)Ketonların indirgenmesinden sekonder alkoller oluşur.
Su katılmasıKetonlara su katılmasıyla kararsız keto hidrat bileşikleri oluşur.
Ketonların en küçük üyesi olan asetonun kondensasyonundan aromatik bir bileşik olan mezitilen meydana gelir.
Kondensasyon Birden fazla küçük moleküllerin polimerleşme sırasında, küçük polar moleküllerin ayrılması olayına denir.
Ketonların Eldesi
Sekonder alkollerin bir kademe yükseltgenmesinden ketonlar elde edilir.
Karboksilli asit tuzlarının ısıtılmasından ketonlar elde edilir.
Alkinlere su katılmasından ketonlar elde edilir.
Aldehit ve ketonlarda İzomeri
Aynı C sayılı aldehitlerle ketonlar birbirinin izomeridir. Kapalı formülleri CnH2nO dur.
Propanon ve propanal kapalı formülleri C3H6O olduğundan birbirinin izomeridir.
KARBOKSİLLİ ASİTLER
Bu dersimizde Karboksilli asitler ve genel özelliklerini ele alacağız. İyi dersler…
Yapılarında karboksil 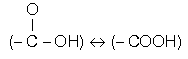 grubu bulunduran bileşiklere karboksilli asitler denir.
grubu bulunduran bileşiklere karboksilli asitler denir.
Karboksilli Asitler
a. Yapısında bulundurdukları —COOH grubu sayısına göre:
1. Mono karboksilli asitler
Yapılarında 1 tane —COOH grubu bulunduranlar
2. Poli karboksilli asitler
Yapılarında birden fazla —COOH grubu bulunduranlar.
2 tane —COOH grubu bulunduranlara di karboksilli asitler 3 tane —COOH grubu bulunduranlara tri karboksilli asitler adı verilir.
b. Yapılarında —OH ya da —NH2 bağlı olanlar
1. —COOH grubu yanında —OH grubu da bağlı ise oksi asitler adı verilir.
2. —COOH grubu yanında —NH2 grubu da bağlı ise amino asitler adı verilir.
Mono karboksilli asitlerin genel formülleri  şeklindedir. CnH2nO2 kuralına uyar.
şeklindedir. CnH2nO2 kuralına uyar.
İsimlendirme yapılırken aynı sayıda karbon u bulunduran alkanların sonuna “oik asit” eki getirilir.
R grubu dallanmış bir hidrokarbon ise, karboksil grubunun bulunduğu karbon una birinci karbon numarası verilerek diğerleri numaralandırılır.
Ayrıca COOH grubundan sonraki 2. karbon una a, 3. karbon una b, 4. karbon una g harfleri verilerek de isimlendirme yapılır.
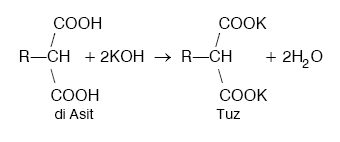
Poli asitler ise şöyle isimlendirilir;

Karboksilli Asitlerin Genel Elde Edilişleri
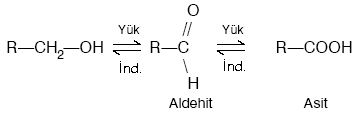
1. Primer alkollerin iki derece yükseltgenmesinden
Primer alkoller bir derece yükseltgenirse aldehitler oluşur. Aldehitler yükseltgenirse karboksilli asitler oluşur. Yani primer alkoller 2 kademe yükseltgenirse karboksilli asitler oluşur.
2. Grignard Bileşiklerinden

3. Karboksilli Tuzlarından
R—COONa + HBr ® R—COOH + NaBr
Karboksilat Tuz Karboksilli Asit
Karboksilli Asitlerin Özellikleri ve Reaksiyonları
- Karboksilli asitlerin molekülleri arasında dihidrojen bağı vardır. Bundan dolayı aynı karbon sayılı, eter, aldehit, keton ve alkollerden daha yüksek sıcaklıkta kaynarlar.
- Su ile hidrojen bağı oluşturabildiklerinden suda kolayca çözünürler. Ancak zayıf asit olduklarından suda az iyonlaşırlar. Molekül ağırlığı arttıkça iyonlaşma % leri azalır.
- Homolog sıra oluşturabilirler.
- Aktif metallerle H2 gazı açığa çıkarırlar.
Alkoller yalnızca K ve Na gibi metallerle tepkime verirler. Asitler ise K, Na, Mg, Zn…… gibi metallerle de tepkime verirler. Bu özellik Karboksilli asitleri alkollerden ayırır.
R—COOH + Na ® R—COONa +
H2
K. asit Tuz
2R—COOH + Ca ® (R—COO)2 Ca + H2
Karboksilli asitler, bazlarla nötürleşme tepkimesi verirler.
R—COOH + NaOH ® R—COONa + H2O
Asit Tuz
Karboksilli asitler, karbonatlı (Na2CO3, MgCO3…) tuzlarla tepkime verirler.
2R—COOH+CaCO3 ® Ca(R—COO)2(g) + CO2 + H2O
Asitin karboksil grubundaki OH grubu çıkarılırsa kalan kısma açil grubu denir.
Karboksilli asitler, alkollerle esterleri oluştururlar.
Yağ Asitleri
Yağ asitleri çift ve yüksek karbon sayılı karboksilli asitlerdir.
Doymamış yağ asiti dendiğinde alkil grubunda en az bir tane çift bağ bulunduran yağ asitleridir. Bu asitler oda sıcaklığında sıvı haldedir.
NOT: Adipik asidin hegzametilen diamin ile kondensasyonu sonucu naylon oluşur. OPTİKÇE AKTİFLİK
Bir C atomuna 4 farklı ya da grup bağlı ise bu C atomuna asimetrik C atomu adı verilir. Molekülde asimetrik C atomu bulunduran bileşikler optikçe aktif maddelerdir. Bu maddeler polarize ışığın titreşim düzlemini çevirirler.
Yukarıdaki bileşiklerde yıldız konulan C atomları asimetrik C atomu’dur.
ESTERLER
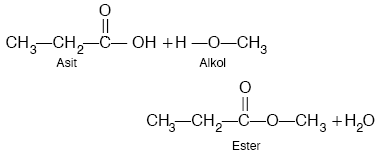
Bir mol karboksilli asitle, bir mol mono alkol tepkimeye girerse 1 mol ester ve 1 mol su oluşur. Bu olaya esterleşme olayı denir.
İsimlendirme
Asit adı, alkolden gelen alkil adı ve esteri sözcüğü okunarak
Alkolden gelen alkil grubunun adı yazılır, sonra asitin “oik asit” kısmı kaldırılır.
Yerine -at eki getirilir.Esterlerin Elde Edilişi ve Reaksiyonları
Karboksilli asitlerin, asidik ortamda alkollerle tepkimesinden ester elde edilir.
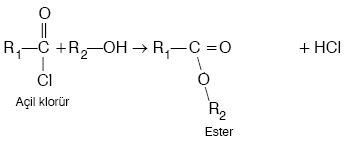
Acil klorürlerin alkollerle tepkimesinden esterler elde edilir.
Esterler eşit C atomlu karboksilli asitlerle izomerdir.
Yağlar
Yağ asitlerinin gliserin ile oluşturdukları esterlerdir. Bunlara gliseridde denir. Kullanılan yağ asidi doymuş ise katı yağlar, asit doymamış ise sıvı yağlar elde edilir. Sıvı yağlar H2 ile doyurularak katı yağlar (Margarin) elde edilir. Mumlar ise ester, alken, aldehit karışımlarıdır.
Sabunlaşma
Büyük moleküllü karboksilli asitlerin Na ve K tuzlarına sabun denir.
Karboksilli asitlerin gliserin ile tepkimesinden ester elde edilir.
Esterlerin (yağların) bazik ortamdaki hidrolizine sabunlaşma denir.
NOT: Deterjanların sabunlardan daha iyi temizleyici olması, sert suda dahi çözünebilmesindendir.
ALİFATİK AMONYAK TÜREVLERİ
AMİNLER
Amonyakdaki hidrojen atomlarının yerine Alkil gruplarının bağlanmasıyla aminler oluşur.
Aminler isimlendirilirken alkil gruplarından sonra amin kelimesi getirilir.
Aminler zayıf baz özelliği gösterirler. Suda OH– iyonu vererek iyonlaşırlar.
CH3 – NH2 + H2O ® CH3 NH3+ + OH–
Aminler asitlerle reaksiyona girerek tuz oluştururlar.
CH3 – NH2 + HCI ® CH3 – NH3CI
AMİNO ASİTLER
Molekülünde hem karboksilli asit (–COOH), hem de amin (–NH2) grubu bulunduran bileşiklerdir.
Basit primer ve sekonder aminler amonyaktan daha kuvvetli anhidrobazlardır. Tersiyer aminlerde bazlık özelliği daha küçüktür.
Amino asitler, moleküllerinde hem asidik (karboksil grubu), hem de bazik (amino grubu) gruplar bulundurduğundan anfoter bileşiklerdir.
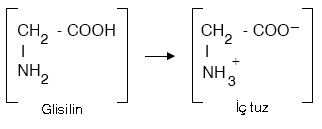
Amino asitlerdeki karboksil hidrojeninin –NH2 grubuna geçmesiyle iç tuz oluşur.
Amino asitler anfoter olduklarından hem asitlerle hem de bazlarla tuz oluştururlar.
Amino asitler proteinlerin yapı taşlarıdır.
AMİTLER
Karboksilli asitlerdeki karboksil grubunun,
‘ ı yerine NH2 grubunun bağlanmasıyla amitler oluşur.
Primer amitler karboksilli asitler gibi isimlen-dirilir. Karboksilli asitteki – OİKASİT eki yerine –AMİT kelimesi getirilir.
Sekonder ve tersiyer amitler, primer amit gibi isimlendirilir. Azota bağlı gruplar (N–) yazılıp belirtilir.
Amitler nötr özellik gösterirler.
Amitler genellikle suda çözünürler.
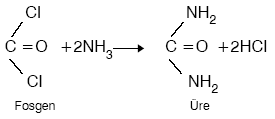
DİAMİT (ÜRE)
Üre idrarda bulunur. İdrardan elde edildiği gibi sentetik olarak da elde edilir. Azot gübresi olarak kullanılır. Suda çok, alkolde az çözünür.
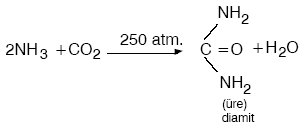
Üre, NH3 ve CO2‘nin yüksek basınçta ısıtılmasından elde edilir.
Üre, fosgenin NH3 ile etkileşmesinden elde edilir.
KARBONHİDRATLAR
Genel formülleri Cn(H2O)m şeklinde olan bileşikler karbonhidratlardır.
Günlük hayattaki yiyeceklerin büyük bölümü (unlu ve şekerli besinler) ile giyeceklerin bir kısmı (pamuklu, ketenli, suni ipekli karbonhidratlar) yeşil bitkiler tarafından fotosentez yoluyla üretilir. Yeşil bitkilerin kökleriyle topraktan aldıkları su ve yapılarındaki gözenekleriyle havadan aldıkları karbondioksiti yapraklarındaki klorofilin katalizörlüğünde güneş enerjisinden yararlanılarak karbonhidrat haline dönüştürülür. Bu olaya fotosentez denir.
6CO2 + 6H2O ® C6 (H2O)6 + 6O2
Glikoz
Karbonhidratlar formaldehitin polimeri gibi düşünülebilir. Karbonhidratları, yapılarında aldehit veya keton grubu bulunduran poli alkoller olarak tanımlayabiliriz.
Yapılarında aldehit bulunduranlara aldoz, keton bulunduranlara ketoz denir.
Karbonhidratların sınıflandırılması
Mono sakkaritler : Glikoz, fruktoz galaktoz
Di sakkaritler : Sakkaroz, sükroz, laktoz
Poli sakkaritler : Selüloz, nişasta, glikojen
Mono Sakkaritler
Basit şekerlerdir. Tatlı olup suda çözünürler. Glikoz, galaktoz, fruktoz mono sakkaritlere örnektir. Mono sakkaritler optikçe aktiftir.
Glikoz, yapısındaki aldehit grubundan dolayı tollens ayıracı ve fehling çözeltisi ilereaksiyon verir.
Fruktoz, ise yapısında keton grubu olmasına rağmen halkalı yapıya döndüğünde a – hidroksi yapı kazandığı için diğer ketonlardan farklı olarak tollens ve fehling ile reaksiyon verir.
Di Sakkaritler
İki molekül mono sakkaritten 1 mol su çekilmesiyle di sakkaritler oluşur.
Glikoz + Glikoz ® Maltoz
Glikoz + Fruktoz ¾¾® Sakkaroz
–H2O
Glikoz + Galaktoz ® Laktoz
C6H12 O6 + C6 H12 O6 ¾¾® C12 H22 O11
–H2O
Günlük hayatta kullanılan maltoz (meyve şekeri), sakkaroz (çay şekeri) ve laktoz (süt şekeri) birer di sakkarittir.
Poli Sakkaritler
Günlük hayatta nişasta, dekstrin, selüloz ve türevleri olarak kullanılan maddeler birer poli sakkaritlerdir.
n molekül mono sakkaritden, (n–1) molekül su çıkarılmasıyla poli sakkaritler oluşur.
Molekül sayısı 5 – 15 ise dekstrin, 20 ise glikojen, 30–35 ise Nişasta ve 2000 kadar ise selüloz meydana gelir.
AROMATİK BİLEŞİKLER
Açık yapılı (halkasız) bileşiklere alifatik dendiğini söylemiştik. Halkalı yapıda olan bileşiklerden bazıları aromatik özellik gösterirler.
Bir organik bileşiğin aromatik olduğunu anlamak için aşağıdaki özelliklere bakmak gerekir.
- Halkalı yapıdadırlar.
- Halkadaki bağlar tek, çift, tek, çift olmak üzere dönüşümlü ile sıralanmıştır.
- Halkadaki p elektronları sayısı;
(4n + 2) olmalıdır. (n : halka sayısı)
Yukarıdaki özellikleri gösteren bileşikler aromatiktir.
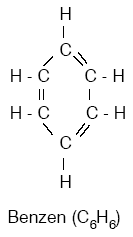
Aromatik bileşiklerin en küçük üyesi benzendir. Kapalı formülü C2H2 olup CnH2n–6 genel formülü ile gösterilir. Benzende C atomları arasında üç tane çift bağ vardır. Çift bağlar tek-çift-tek-çift şeklinde sıralanmıştır. Benzende 6 karbonlu bir halka vardır.
Benzen doymamış bir hidrokarbon olmasına rağmen doymamış hidrokarbonların özelliklerini göstermez. Katılma reaksiyonu vermez. Yer değiştirme reaksiyonu verir.
Benzen molekülü aşağıdaki şekillerde de gösterilir.
Benzen halkasından hidrojen çıkmasıyla geriye kalan köke FENİL denir. Aşağıdaki şekillerde gösterilir.
BENZENİN TÜREVLERİ
BENZENİN MONO TÜREVLERİ
Benzendeki hidrojenler, halkanın elektronca zengin olması sebebiyle katyon hale geçmeye elverişlidirler. Benzen halkasına katyon hale getirilmiş veya gruplarla saldırı başlatılırsa H+ kopması ile birlikte grup halkaya yerleşmiş olur. Olay yerdeğiştirme reaksiyonudur. Sonuçta benzen türevleri elde edilir.
Benzen molekülünden bir hidrojen çıkıp yerine bir ya da fonksiyonel grubun bağlanmasıyla benzenin mono türevleri oluşur. Benzenin mono türevlerinin bir tane izomeri vardır.
Benzenin mono türevleri adlandırılırken halkaya bağlı grubun adından sonra benzen eki getirilir.
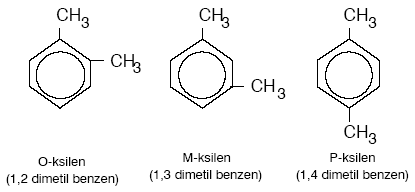
BENZENİN Dİ TÜREVLERİ
Benzen molekülünden iki hidrojen u çıkarılıp yerine yada gruplarının bağlanmasıyla benzenin di türevleri oluşur.
“Orto” “meta” “para” olmak üzere üç tane izomeri vardır. Grupların birbirini takip eden karbonlara bağlanması halindeki izomeri orto, bir atlayarak karbonlara yerleşmesi meta, karşılıklı karbon larına yerleşmesi halindeki izomeri para olarak isimlendirilir.
BENZENİN TRİ TÜREVLERİ
Benzen halkasından üç hidrojen u çıkarılıp yerine ya da gruplarının bağlanmasıyla benzenin tri türevleri oluşur.
Visinal, simetrik, Asimetrik olmak üzere üç izomeri vardır.
BAZI AROMATİK BİLEŞİKLER
Toluen (Metil benzen) Benzendeki H inin —CH3 ile yer değiştirme-sinden elde edilir. FENOL (OKSİ BENZEN)
Zayıf asit özelliği gösterir. Sulu çözeltisi FeCI3 ile mor renk verir. Bu fenolün tanınma reaksiyonudur. BENZİL ALKOL
Aromatik bir alkoldür. Alifatik alkollerin özelliklerini gösterir. BENZALDEHİT
Aromatik aldehittir. Bazı reaksiyonları alifatik aldehitlere benzer. Yükseltgendiğinde karboksill asit oluşur. Fehling ayıracına etki etmez. Amonyaklı gümüş nitrata zor etki eder. Zayıf indirgendir. AMİNO BENZEN (ANİLİN)
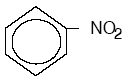
Aromatik bir amin bileşiğidir. Zayıf baz özelliği gösterir. NİTRO BENZEN
Benzenin derişik nitrik asit ve derişik H2SO4 karışımı, ile reaksiyonundan elde edilir. HNO3 + 2H2SO4 NO2+ + H3O+ + 2HSO4–
TRİ NİTRO TOLUEN (TNT)
(2,4,6 Trinitro toluen)
TNT patlayıcı özelliktedir. Trotil adıyla top mermileri, deniz ve kara mayınlarını doldurmakta kullanılır.





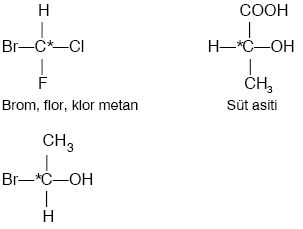
















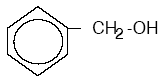








Hiç yorum yok
Sizleri daha ilerilere taşıyabilmek için burdurdayız